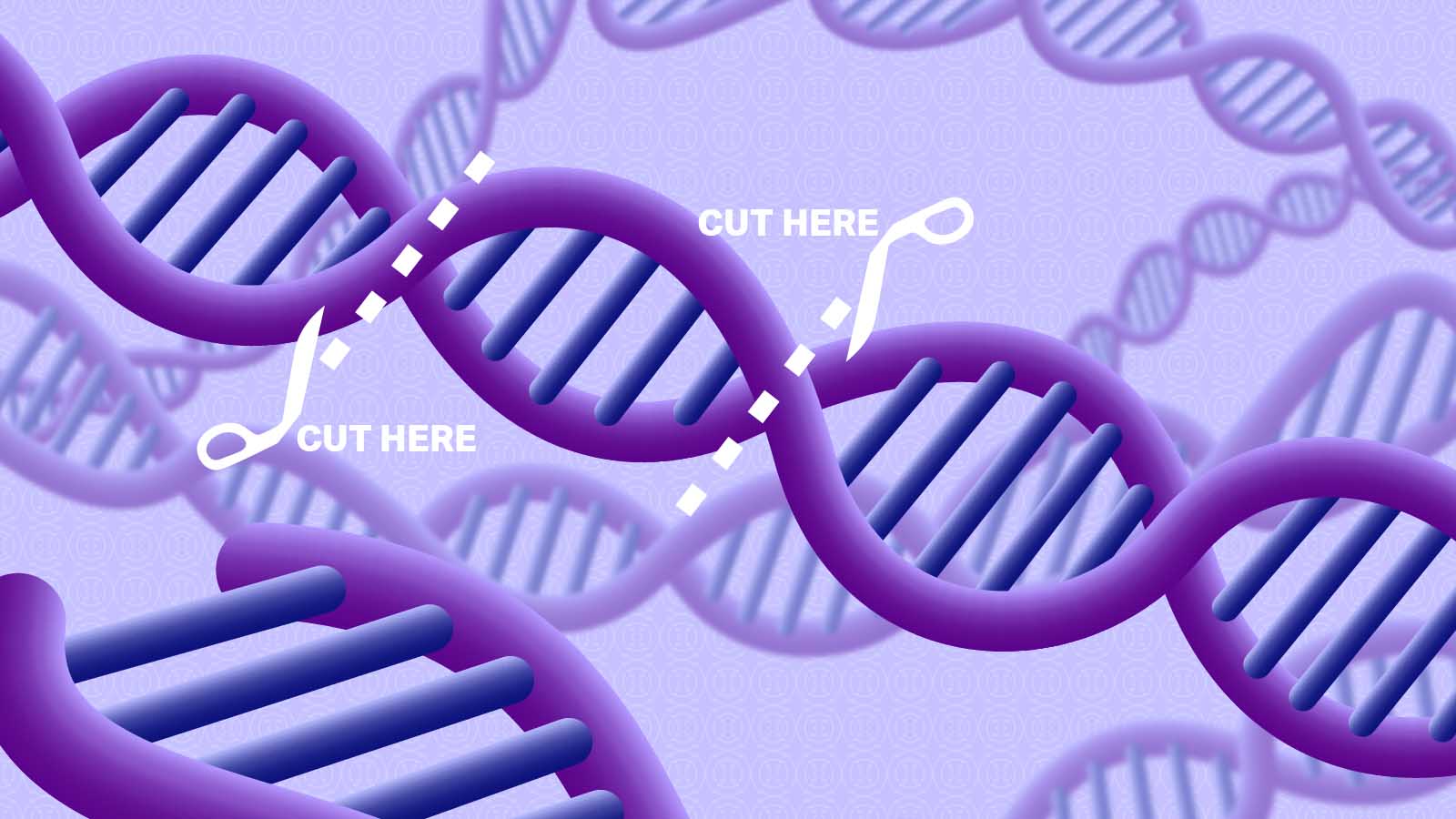
CRISPR là gì?
CRISPR là một phương pháp hiện đại, công nghệ cao để chỉnh sửa gen, nhưng nó dựa trên nền tảng hệ thống bảo vệ tự nhiên đơn giản có ở nhiều vi khuẩn.
Giống như các sinh vật bậc cao, vi khuẩn cũng phải đương đầu với một số loại virus và plasmid có thể xâm nhập và tiêu diệt chúng. Vi khuẩn duy trì một “thư viện di truyền” bên trong DNA của chúng, “thư viện” chứa các đoạn gen quan trọng từ các cuộc chạm trán với “mầm bệnh của chúng” trong quá khứ và với những mầm bệnh mà chúng thường xuyên phải đối mặt.
CRISPR là chữ viết tắt từ những chữ cái đầu tiên của cụm từ “Clustered Regularly Interspaced Short Palindromic Repeats” (tạm dịch là: tập hợp các trình tự DNA ngắn xuôi ngược lặp lại – tức là đọc theo hướng xuôi hay ngược thì đều có trình tự DNA giống nhau và bằng nhau), về cơ bản đây là thứ mà các “thư viện” của vi khuẩn sử dụng để lập danh mục các mối đe dọa virus và plasmid khác nhau.
Các trình tự này, kết hợp với các enzym đặc biệt, có thể đóng vai trò như các “chiếc kéo” săn lùng và cắt chính xác các DNA hoặc RNA để tiêu diệt những kẻ xâm lược nội bào trước khi chúng có thể tái tạo và nhân lên. Mẹo để tránh bất kỳ thiệt hại nào tự gây ra (tức tự cắt DNA hoặc RNA của chính vi khuẩn) đối với trình tự di truyền trong thư viện của vi khuẩn là ngoài trình tự di truyền virus cụ thể, chiếc kéo cũng tìm kiếm cái được gọi là “mô típ liền kề nằm cạnh vùng đệm” (PAM - protospacer adjacent motif), được tìm thấy trong vật chất di truyền của kẻ xâm lược nhưng không có trong vi khuẩn.

Hình của https://www.vinmec.com
Một khi các nhà khoa học học được cách lập trình của “những chiếc kéo phân tử CRISPR” bằng cách sử dụng trình tự di truyền được thiết kế riêng của họ thay vì trình tự từ thư viện của vi khuẩn, họ có thể nhắm mục tiêu đến các điểm cụ thể trên DNA để “tắt” hoặc "loại bỏ" một số gen nhất định ở hầu hết mọi sinh vật. Loại nghiên cứu này vẫn được thực hiện ở nhiều loài thủy sinh, đặc biệt là đối với các vấn đề về sức khỏe và khả năng miễn dịch.
Tuy nhiên, sau một thời gian ngắn nghiên cứu mang tính chất tìm hiểu, khám phá dựa trên phương pháp tiếp cận là “đập nó ra rồi xem điều gì sẽ xảy đến”, một số ứng dụng thiết thực đã bắt đầu xuất hiện.
Tuy nhiên, nếu các sửa đổi từ việc chỉnh sửa gen có thể di truyền, chúng thường phải được thực hiện từ giai đoạn rất sớm trong quá trình phát triển của động vật hoặc thực vật (lý tưởng nhất là ở giai đoạn một tế bào), từ đó nó có thể được kết hợp trong các giao tử khi trưởng thành.
Với cách tiếp cận này, nảy sinh nhu cầu về các phương pháp chuyên biệt như vi tiêm để cung cấp các cấu trúc CRISPR và các enzym ở quy mô siêu nhỏ. Một tác dụng phụ khó chịu của phương pháp này là hiệu ứng CRISPR có thể tiếp tục trong phôi thai đang phát triển vượt xa giai đoạn một tế bào, thường dẫn đến hiện tượng thể khảm (mosaicism - các tế bào khác nhau hiển thị các cấu tạo di truyền khác nhau).
Đánh giá khoa học và chi tiết từng bước về cách CRISPR đã phát triển vượt quá phạm vi của bài viết này, nhưng đủ để nói rằng các ứng dụng tiềm năng cho công nghệ này dường như chỉ đang ở giai đoạn hạn chế bởi trí tưởng tượng của các nhà khoa học đã làm chủ nó. Một số ví dụ bao gồm việc thay đổi muỗi để chúng không thể tìm thấy mục tiêu của con người, lai tạo hạt cà phê với tất cả hương vị và không chứa caffeine, phát triển rượu vang không gây nôn có lợi cho sức khỏe, tạo ra cà chua có cùng gen sản xuất gia vị như ớt (gen này đã tồn tại, chỉ là không biểu hiện), phân tích phân tử để tìm mầm bệnh trong môi trường tự nhiên hoặc nhân tạo và thậm chí mang trở lại loài voi ma mút đã tuyệt chủng.

Hình cà chua chỉnh sửa gen bằng công nghệ CRISPR có chứa hàm lượng cao axit gamma-aminobutyric (GABA), một loại axit amin được cho là giúp thư giãn và giúp giảm huyết áp cao gấp 4 - 5 lần so với cà chua thông thường. Nguồn: https://www.isaaa.org - Japan Launches World's First Genome-Edited Tomato, March 24, 2021
Những gì đã được thực hiện cho đến nay?
Cho đến nay, hầu hết các nghiên cứu về CRISPR ở các sinh vật thủy sinh nuôi đều phản ánh những nỗ lực tương tự như các sáng kiến cải tiến di truyền truyền thống hơn, đó là tăng trưởng, kháng bệnh và vô sinh, mặc dù một số nghiên cứu thú vị cũng đã được thực hiện liên quan đến các kiểu màu sắc ở các loài cá khác nhau.
Các vấn đề khi áp dụng công nghệ cho các đặc điểm phức tạp như tăng trưởng và kháng bệnh vẫn còn, vì một số gen có liên quan và nhiều gen trong số đó có thể yêu cầu chỉnh sửa để đạt được kết quả mong muốn. May mắn thay, những tiến bộ trong việc chọn lọc bộ gen vẫn tiếp tục ở nhiều loài thủy sản và điều này có thể cung cấp các con đường tắt cho việc áp dụng CRISPR, nhưng sẽ cần nhiều công việc quan trọng để xác định phiên bản của gen nào nên được nhắm mục tiêu thông qua chỉnh sửa.
Hiện có thể chỉnh sửa để chèn các alen nhân tạo hoặc trình tự di truyền từ các loài khác, nhưng rất có thể sẽ phải đối mặt với sự phản ứng đối với việc thương mại hóa các sinh vật thủy sinh chuyển đổi gen.
Ở cá hồi, phần lớn công việc cho đến nay là tập trung vào cá hồi Đại Tây Dương. Trong khi CRISPR có thể được sử dụng để sản xuất cá hồi vô sinh bằng cách nhắm vào “dead-end gene”, sẽ cần nhiều nỗ lực hơn để áp dụng phương pháp này về mặt thương mại vì nó không thể được truyền sang các thế hệ tiếp theo.
Tuy nhiên, các nghiên cứu trước đây với các loài trong phòng thí nghiệm (cá ngựa vằn và cá medaka) cho thấy rằng một phương pháp để khôi phục khả năng sinh sản cho đàn giống có thể khả thi. Trong một nghiên cứu khác, “dead-end gene” đã được sử dụng để tạo ra cá vô sinh, sau đó có thể được cấy với tế bào mầm từ cá hiến tặng có quan hệ họ hàng gần (loài có nguy cơ tuyệt chủng hoặc có giá trị thương mại hơn). Một ví dụ ở Nhật Bản liên quan đến việc sử dụng cá nóc sao đã qua chỉnh sửa (Takifugu alboplumbeus) để làm cá thể bố mẹ thay thế cho loài cá nóc hổ có giá trị cao hơn (T. rubripes).
.jpg)
Cá nóc sao - Nguồn https://www.inaturalist.org

Hình cá nóc hổ - Nguồn: https://www.123rf.com
Tăng cường khả năng chống lại các mầm bệnh khác nhau có vẻ như là mảnh đất màu mỡ để ứng dụng CRISPR trong nuôi trồng thủy sản, nhưng khả năng kháng bệnh là một hiện tượng phức tạp liên quan đến sự tương tác của các loài vật chủ với cả mầm bệnh và môi trường nuôi, cũng như nhiều gen có liên quan khác. Một nghiên cứu quan trọng khác có nhiều hứa hẹn về mặt thương mại liên quan đến việc xác định các gen có khả năng chống lại rận biển ở các loài cá hồi Thái Bình Dương và sau đó thiết lập các thuộc tính tương tự ở cá hồi Đại Tây Dương thông qua chỉnh sửa gen.
Hồi 2018, các nhà nghiên cứu Nhật Bản đã báo cáo về việc sử dụng kỹ thuật CRISPR để phát triển dòng cá tráp biển đỏ với khối lượng cơ bắp được gia tăng nhiều hơn và chiều dài cơ thể tương đối ngắn. So với cá tráp không được chỉnh sửa gen, dòng này cho thấy lượng cơ ăn được tăng 16%, và trong vòng hai năm, một quần thể nhân giống ổn định đã được thiết lập.
Như trường hợp của nhiều nỗ lực khác đối với các loài nuôi trồng thủy sản, công trình này được xây dựng dựa trên nghiên cứu trước đó về các quần thể cá ngựa vằn và cá mekada trong phòng thí nghiệm. Hai năm sau, các nhà khảo sát Trung Quốc báo cáo về một dòng cá lăng vàng (Pelteobagrus fulvidraco) cũng được sản xuất thông qua chỉnh sửa gen myostatin. 210 ngày sau thụ tinh, cá từ dòng đã chỉnh sửa nặng hơn 37% so với cá chưa chỉnh sửa gen.
Việc chỉnh sửa gen myostatin cũng đã được báo cáo làm tăng đáng kể khối lượng cơ ở cá chép, cá bơn ô liu, cá tráp mõm cùn, cá tráp biển, chạch bùn và cá da trơn trong 5 năm qua và các nhà khoa học hiện đang bắt đầu xem xét các gen khác trong nỗ lực tăng cường tốc độ tăng trưởng ở các loài thủy sản.
Trong vài tháng qua, một nhóm các nhà nghiên cứu khác từ Trung Quốc đã báo cáo về việc sử dụng CRISPR để loại bỏ gen PI3K ở cá chép Gibel. Sự gián đoạn của gen này giúp cải thiện độ nhạy insulin ở động vật có vú, nhưng cá chép đã qua chỉnh sửa không biểu hiện sự thay đổi hay hấp thu hoặc hấp thu glucose trong huyết tương và gan. Tuy nhiên, chúng đã cải thiện sự tăng trưởng của tế bào soma và hiệu quả chuyển đổi thức ăn. Một nghiên cứu khác gần đây ở Trung Quốc đã xác định rằng việc loại bỏ gen t1r1 đã cải thiện đáng kể sự chấp nhận protein thực vật ở cá ngựa vằn.

Hình cá chép Gibel
Màu sắc và các kiểu màu cũng là những cân nhắc quan trọng ở một số loài nuôi trồng thủy sản. Tại Trung Quốc, các nhà nghiên cứu đã sử dụng CRISPR để phá vỡ các gen vận chuyển carotenoid nhằm làm thay đổi các kiểu màu đỏ và trắng ở cá chép cảnh.
Một nhóm khác đã sử dụng công nghệ để thay đổi hai gen protein truyền tín hiệu agouti (ASIP) để loại bỏ các mảng đen ở cá chép Oujiang. Cũng tại Trung Quốc, trong một nghiên cứu sắp được công bố, các nhà nghiên cứu đã sử dụng CRISPR để loại bỏ gen tyrosinase trong dòng cá rô phi đỏ (điêu hồng). Một khi một quần thể sinh sản thực sự được thiết lập, việc sản xuất liên tục những con cá rô phi đỏ đồng đều và không có sắc tố đen là có thể thực hiện. Và các nhà khoa học Israel gần đây đã công bố kết quả (trên Tạp chí CRIPSR) chi tiết việc sử dụng CRISPR để tạo ra cá rô phi Nile bạch tạng thực sự (mắt hồng). Họ đã phá vỡ gen slc45a2, gen trung gian sinh tổng hợp melanin, để tạo ra hợp tử có tới 99% bạch tạng, bao gồm cả việc thiếu sắc tố melanin ở mắt.
Các nhà khoa học Trung Quốc cũng đã dùng kỹ thuật CRISPR trên tôm ridgetail white prawn (Exopalaemon carinicauda). Các loài giáp xác khác đã được biến đổi thành công bằng cách sử dụng CRISPR bao gồm Daphnia magna và giáp xác mềm amphipod Parhyale hawaiensis.
Hình tôm gai ridgetail white prawn (Exopalaemon carinicauda)
Để tiếp cận chiến lược dựa trên CRISPR, cần có một số kiến thức về bộ gen của sinh vật. Mặc dù rất ít và còn xa vời, nhưng một số bộ gen của nhuyễn thể hai mảnh vỏ hiện có sẵn cho loại nghiên cứu này, gồm các bộ gen của hàu Thái Bình Dương, hàu đá Sydney, vẹm Địa Trung Hải, sò điệp, ….. Tuy nhiên, cho đến nay công việc chỉnh sửa gen của nhuyễn thể hai mảnh vỏ khá khó khăn. Các nhà nghiên cứu đã báo cáo về việc sử dụng CRISPR nhắm vào gen myostatin ở hàu Thái Bình Dương đã có một số thành công khi sử dụng phương pháp vi tiêm.
Nhìn về phía trước
Hiện tại, việc áp dụng CRISPR cho các loài thủy sinh sẽ tiếp tục là mục tiêu theo đuổi của các tổ chức nghiên cứu và học thuật. Đối với trường đại học là để phát triển công nghệ phân tử và chuyên môn cần thiết, nhưng đối với tư nhân, mối quan tâm là thiết lập năng lực công nghệ cao như vậy, thì cần phải đầu tư rất nhiều vào thiết bị và nhân viên. Tuy nhiên, CRISPR rẻ hơn và chính xác hơn các lựa chọn chỉnh sửa gen thay thế khác và thường mang lại kết quả tốt hơn.
Các ứng dụng và ý nghĩa trong tương lai đối với nghiên cứu liên quan đến CRISPR cho các loài nuôi trồng thủy sản hiện đang được tranh luận, đôi khi rất sôi nổi, trong nhiều bối cảnh khoa học và xã hội.
Một điều mà chúng ta có thể chắc chắn là sự tiến bộ về hiểu biết của chúng ta đối với bộ gen và các tương tác sinh lý phức tạp của nhiều loài thủy sản quan trọng, do đó sẽ cho phép việc chỉnh sửa gen nhắm tới các mục tiêu chính xác hơn nhằm cải thiện các đặc tính sản xuất. Và tất cả đều có khả năng giảm thiểu thực sự các tác động di truyền đối với các loài thủy sản hoang dã.
Theo https://thefishsite.com
Lược dịch bởi: KS. Nguyễn Thành Quang Thuận - VPAS JSC